周俊主任:相关靶点及基因突变的胃/食管癌的免疫、靶向治疗联合化疗策略的探讨(2021 BOC/BOA 精彩回顾|)
2021年7月2日,中国临床肿瘤学会(CSCO)联合北京市希思科临床肿瘤学研究基金会共同主办的“2021年中国临床肿瘤学年度进展研讨会(BOC)暨BestofASCO®2021China”在成都顺利召开。
大会围绕2021年美国临床肿瘤学会(ASCO)年会“无时无刻,无微不至”的主题,依据国内肿瘤的发病情况,邀请国内多领域肿瘤学专家分别就2021ASCO会议中的精彩研究进行点评报告;其中高博医学阿特蒙肿瘤中心首席科学家李进教授担任大会主席,高博医学阿特蒙肿瘤中心周俊主任围绕本届ASCO年会中胃癌领域摘要号为4010、4013两项研究展开报告,总结在胃癌领域BOA研究聚焦在相关靶点及基因突变的胃/食管癌的免疫、靶向治疗联合化疗策略的探索。

HER2是人表皮生长因子受体-2的缩写,实际上是一种原癌基因,临床上胃癌可按HER2检测分为阴性和阳性两种,HER2阳性胃癌是胃癌的一种分子亚型,该类患者预后差,接受标准化疗方案后疾病控制时间不超过6个月。ToGA研究结果证实,曲妥珠单抗联合化疗可显著延长HER2阳性转移性胃癌(mGC)患者的总生存期超过1年。今年5月,FDA批准Keytruda(帕博利珠单抗)联合曲妥珠单抗和含氟嘧啶及铂类化疗用于局部晚期不能切除或转移性HER2阳性的胃/食管连接部腺癌患者的一线治疗。
「免疫+靶向+化疗」胃癌三联疗法获FDA加速获批,总缓解率高达74%
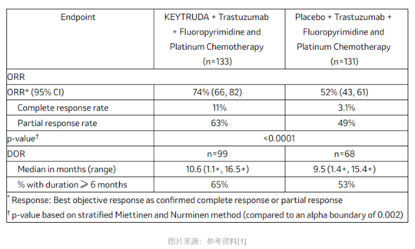
此次获批是基于KEYNOTE-811的Ⅲ期临床试验的研究结果。周俊主任在会议上分享了该研究:入组了先前未曾接受过针对转移性疾病治疗的HER2阳性晚期胃或胃食管结合部腺癌患者,且患者按1:1的比例随机分配,接受帕博利珠单抗或安慰剂联合曲妥珠单抗和化疗方案。

数据显示
帕博利珠单抗组的总缓解率(ORR)为74%,对比对照组的52%,帕博利珠单抗组的总缓解率ORR提升了22%;
帕博利珠单抗组的中位反应持续时间(DOR)为10.6个月,而对照组为9.5个月[1]。
帕博利珠单抗+曲妥珠单抗+化疗:1+1+1>3
帕博利珠单抗在2017年9月就被FDA获批用于PD-L1阳性的复发性局部晚期或转移性胃癌、胃食管结合部腺癌的治疗。
帕博利珠单抗作用机制
T细胞是人体的免疫细胞,能够识别体内的非正常细胞。肿瘤细胞便是属于非正常细胞,通常情况下,T细胞能够自动识别并攻击肿瘤细胞。
但当PD-L1/PD-L2配体与T细胞的表面的PD-1受体相结合时,T细胞便会被其蒙骗,将肿瘤细胞当成正常细胞。如此,T细胞便不会主动攻击肿瘤细胞。
为了让T细胞重新认清肿瘤细胞,PD-1抑制剂如帕博利珠单抗就派上用场。它能够与T细胞的表面的PD-1受体结合,帮助T细胞能够顺利识别肿瘤细胞,并对其进行攻击。
曲妥珠单抗作用机制
曲妥珠单抗是能够精准的识别HER2阳性的肿瘤细胞,当它的一端和肿瘤细胞结合后,另一端会与NK细胞、巨噬细胞等杀伤细胞结合,并诱导杀伤细胞释放出杀伤物质,进而杀死癌细胞。这就是传说中的抗体依赖细胞介导的细胞毒性作用(ADCC)。
了解了这两种药物的作用机制后,那么便来说说帕博利珠单抗能够在HER2阳性患者身上显现出疗效的可能原因:
其一,曲妥珠单抗上调癌细胞PD-L1表达水平,并加强免疫浸润的基因表达特征,从而增加帕博利珠单抗的有效性。
其二,帕博利珠单抗增强曲妥珠单抗的主要杀伤机制——ADCC[2-3]。
Bemarituzumab联合化疗患者的疗效好
会后,周俊主任接受了专业媒体的采访,分享了他对于FGFR靶向药物的研究的观点。近日,一项Bemarituzumab联合mFOLFOX6一线治疗FGFR2b阳性进展期胃癌和胃食管交界部腺癌的II期临床研究被证实,FGFR2b过表达的患者均能从Bemarituzumab联合化疗中获益,而ctDNA+患者获益最明显。在FGFR2b免疫组化阳性且ctDNA阳性的患者中,Bemarituzumab联合化疗更是将疾病进展的风险降低了85%、死亡风险降低90%。
而且,Bemarituzumab安全性良好,主要的不良事件(AE)为口腔炎和干眼症。
参考来源:
[1]FDAApprovesMerck’sKEYTRUDA®(pembrolizumab)CombinedWithTrastuzumabandChemotherapyasFirst-lineTreatmentinLocallyAdvancedUnresectableorMetastaticHER2-PositiveGastricorGastroesophagealJunctionAdenocarcinoma.RetrievedMay5,2021,fromhttps://www.businesswire.com/news/home/20210505006075/en
[2]MeleroI,BermanDM,AznarMA,etal.Evolvingsynergisticcombinationsoftargetedimmunotherapiestocombatcancer[J].NatureReviewsCancer,2015,15(8):457-472.
[3]SavasP,LoiS.Investigatingthepositiverelationshipbetweentumor-infiltratinglymphocytesandtrastuzumabtherapy[J].Immunotherapy,2014,6(7):803-805.






