韩宝惠教授:ALK融合阳性晚期NSCLC的治疗同样需要精准再精准
肺癌治疗发展迅速,靶向治疗引领长期生存
韩宝惠教授:肺癌是最常见的恶性肿瘤,其发病率和死亡率均居我国恶性肿瘤首位。经过数十年的发展,肺癌的治疗已经取得长足的进步。回顾历史长河,肺癌的治疗经历了化疗时代、靶向治疗时代,进入到免疫治疗时代。化疗时代,不可切除晚期NSCLC患者接受传统化疗治疗的疗效不佳,中位OS只有1年左右。
随着对肺癌分子生物学更为深入的研究,肺癌精准治疗快速发展,针对驱动基因阳性的晚期NSCLC患者,靶向治疗明显延长了患者生存时间,改善生活质量。已有研究数据显示,对于ALK融合阳性和ROS1融合阳性晚期NSCLC,给予靶向药物治疗,患者的中位OS达到90个月左右[1-4],靶向治疗引领了肺癌的长期生存。近年来,越来越多靶向治疗药物问世,为肺癌更精准的靶向治疗时代提供可能。
当前肺癌已经进入免疫治疗时代,免疫检查点抑制剂改变了驱动基因阴性晚期NSCLC的治疗格局,让一部分患者实现长期生存。优化免疫治疗方案,探寻免疫治疗生物标志物、更佳获益人群,是未来让更多驱动基因阴性NSCLC患者实现长期生存的重要途径。
ALK融合阳性NSCLC已成为一种慢性病
韩宝惠教授:2007年,日本学者首次在NSCLC中发现EML4-ALK融合基因,后续ALK融合阳性NSCLC被划分为单独的一种肺癌亚型。ALK融合基因被称为“钻石突变”,因为ALK TKI为患者带来了非常长的生存时间,ALK融合阳性NSCLC实际上已经成为一种慢性病。
克唑替尼作为全球shou个获批的ALK TKI,开启了ALK融合阳性NSCLC的靶向治疗时代。由于获批上市时间最长,克唑替尼积累了非常多的研究数据。来自美国、日本、法国的真实世界研究结果显示,一线克唑替尼序贯下一代ALK TKI的“1+2”模式,让ALK融合阳性晚期NSCLC患者的中位OS已经超过7年,达到86~89.6个月[1-3],引领了晚期NSCLC生存基准。
J-ALEX研究OS数据公布,后续治疗选择对生存期的影响同样巨大
韩宝惠教授:Ⅲ期J-ALEX研究的最终OS数据在2021年美国临床肿瘤学会(ASCO)年会上公布。中位随访时间为68.6个月,克唑替尼一线治疗日本ALK融合阳性晚期NSCLC患者的5年OS率达到64.11%,在数值上高于阿来替尼组的60.85%。后续治疗情况分析结果显示,克唑替尼组82.7%的患者后续接受了ALK TKI治疗,其中78.8%的患者进展后将阿来替尼作为二线治疗。阿来替尼组则只有25.2%的患者后续接受ALK TKI治疗[5]。
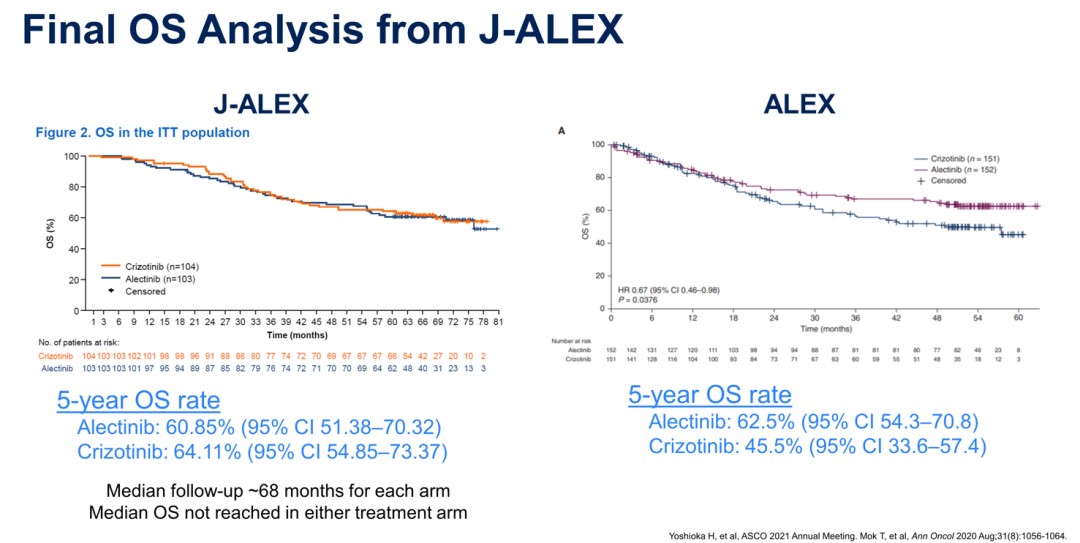
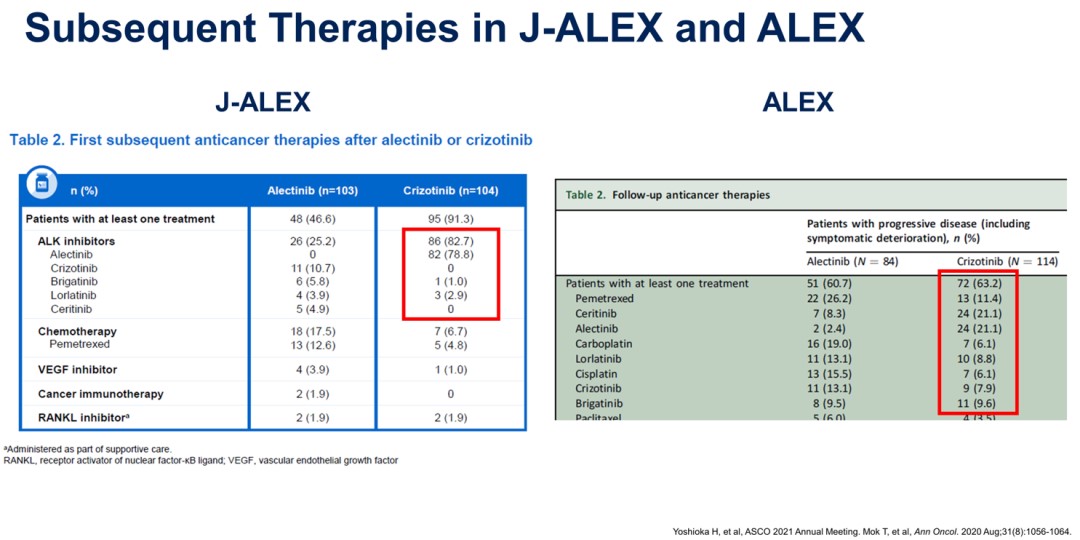
回顾2020年ASCO年会公布的全球多中心、Ⅲ期ALEX研究数据[6],阿来替尼和克唑替尼组的5年OS率分别为62.5%和45.5%,但克唑替尼组患者一线治疗后仅有53.5%的患者后续接受了ALK TKI治疗。综合两项研究的结果可见,阿来替尼5年OS数据相似(60.85%和62.5%),而克唑替尼组则存在较大的差异(64.11%和45.5%),其主要原因是克唑替尼组后续序贯下一代ALK TKI的患者比例存在较大差异(82.7%和53.5%)[5,6]。
从耐药机制层面而言,克唑替尼主要以药理学耐药为主,其次是ALK继发突变和扩增,旁路激活相对少见,序贯下一代ALK TKI可有效解决耐药问题。随着下一代药物在国内可及性越来越高,克唑替尼一线治疗进展后,绝大多数患者均能够接受序贯治疗。
与之相反,第二代ALK TKI主要以继发突变和旁路激活为主,其中G1202R是最常见的继发耐药突变。第二代ALK TKI耐药后治疗选择更加有限,ALEX研究中阿来替尼组只有38.1%的患者后续接受了下一代ALK TKI治疗,而J-ALEX研究序贯ALK TKI治疗的比例则为25.2%。
整体而言,克唑替尼耐药后有更大的机会序贯下一代ALK TKI,从而获得长期生存;而如果将第二代药物放在一线,后续能够序贯其他ALK TKI的比例较低,更多患者可能不得不接受传统化疗。而后续能否序贯ALK TKI治疗,对ALK融合阳性晚期NSCLC患者生存期的影响非常巨大。
药物选择愈加丰富,ALK融合阳性晚期NSCLC的治疗需要更加精准
韩宝惠教授:ALK融合阳性晚期NSCLC是肺癌精准治疗的典范,随着越来越多ALK TKI获批上市,临床医生也面临着治疗选择的问题。除了一线治疗的疗效外,如前文所述,还要更加关注药物耐药机制及后续治疗选择,注重患者的全程管理。
此外,从精准治疗的角度,我们能否通过生物标志物或临床特征的筛选,从而更进一步,为患者提供更加精准和个体化的治疗,例如哪些患者更有机会从“1+2”模式中取得长期生存,哪些患者一线接受第二代ALK TKI后更有机会序贯其他ALK TKI治疗,这可能是未来重要的探索方向之一。
另一方面,EML4-ALK融合基因是最常见的ALK融合类型,而EML4-ALK融合基因又可以进一步细分,目前已经发现了超过17种EML4-ALK变体亚型,其中最常见的V1、V2和V3a/b,占总融合变体的90%[7]。既往有限研究数据显示,与V2、V3a/b患者相比,V1患者接受ALK TKI治疗后的PFS在数值上更高[8,9]。针对不同EML4-ALK变体亚型,给予不同的治疗策略,同样也是精准再精准的研究方向。但由于ALK融合基因的发生率只有5%左右,因此若要进一步细分,开展相关研究,确实也存在不小的阻碍。
【参考文献】
1.Pacheco JM,Gao D,Smith D,et al.Natural History and Factors Associated with Overall Survival in Stage Ⅳ ALK-Rearranged Non-Small Cell Lung Cancer[J].J Thorac Oncol,2019,14(4):691-700.
2.Ito K, Yamanaka T, Hayashi H, et al. Sequential therapy of crizotinib followed by alectinib for non-small cell lung cancer harbouring anaplastic lymphoma kinase rearrangement (WJOG9516L): A multicenter retrospective cohort study[J]. Eur J Cancer, 2021, 145:183-193.
3.Duruisseaux M,Besse B,Cadranel J,et al.Overall survival with crizotinib and next-generation ALK inhibitors in ALK-positive non-small-cell lung cancer (IFCT-1302 CLINALK):a French nationwide cohort retrospective study[J].Oncotarget,2017,8(13):21903-21917.
4.Peled N, Gillis R, Kilickap S, et al. GLASS: Global Lorlatinib for ALK(+) and ROS1(+) retrospective Study: real world data of 123 NSCLC patients[J]. Lung Cancer, 2020, 148:48-54.
5.Yoshioka H, Hida T, Nokihara H, et al. Final OS analysis from the phase Ⅲ j-alex study of alectinib (ALC) versus crizotinib (CRZ) in Japanese ALK-inhibitor naïve ALK-positive non-small cell lung cancer (ALK+ NSCLC)[J]. ASCO 2021, abstract 9022.
6.Mok T, Camidge DR, Gadgeel SM, et al. Updated overall survival and final progression-free survival data for patients with treatment-naive advanced ALK-positive non-small-cell lung cancer in the ALEX study[J]. Ann Oncol, 2020, 31(8):1056-1064.
7.隋泽森, 张建华. EML4-ALK融合基因异形及其相关耐药性的研究进展[J]. 医学综述, 2020, 26(12): 2318-2322.
8.Camidge DR, Dziadziuszko R, Peters S, et al. Updated Efficacy and Safety Data and Impact of the EML4-ALK Fusion Variant on the Efficacy of Alectinib in Untreated ALK-Positive Advanced Non-Small Cell Lung Cancer in the Global Phase Ⅲ ALEX Study[J]. J Thorac Oncol, 2019, 14(7): 1233-1243.
9.Camidge DR, Kim HR, Ahn MJ, et al. Brigatinib Versus Crizotinib in Advanced ALK Inhibitor-Naive ALK-Positive Non-Small Cell Lung Cancer: Second Interim Analysis of the Phase Ⅲ ALTA-1L Trial[J]. J Clin Oncol, 2020, 38(31):3592-3603.






